filmov
tv
DISTRIBUIÇÃO ELETRÔNICA | Resumo de Química para o Enem

Показать описание
Inscreva-se no canal para receber tudo sobre o Enem 100% GRÁTIS
/// SOBRE O VÍDEO
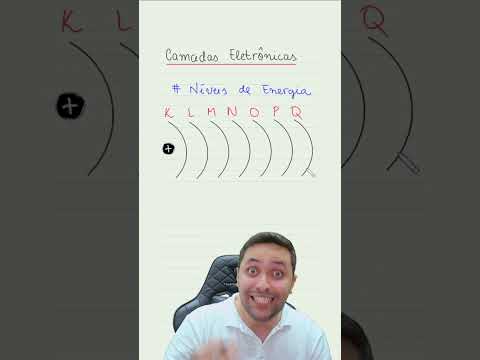
As camadas da eletrosfera representam os níveis de energia da eletrosfera. Assim, as camadas K,L,M,N,O, P e Q constituem os 1º, 2º, 3º, 4º, 5º, 6º e 7º níveis de energia, respectivamente.
Ao longo do tempo, estudos específicos para determinar a energia dos subníveis acabaram mostrando que existe uma ordem crescente de energia nos subníveis. A criação de uma representação gráfica para os subníveis facilitou a visualização da sua ordem crescente de energia. Essa representação é conhecida como diagrama de Linus Pauling.
Nesta aula, o professor Sobis te ensina a fazer a distribuição eletrônica com o diagrama de Linus Pauling. Dúvidas? Deixa nos comentários. ;)
⏱ MINUTAGEM / ASSUNTOS
00:24 a 1:11 - Lembre-se de associar as camadas K, L, M, N, O, P e Q a um número quântico (de 1 a 7). Além disso, vale lembrar que cada uma dessas camadas suporta uma quantidade específica de elétrons, que você confere na lousa.
1:12 a 6:32 - Vocês estão ligados (as) naquela famosa "escadinha" que é o diagrama de Linus Pauling, né? Se liga que agora o prof te ensina a construí-lo de uma forma bem fácil, pra você nunca mais desenhá-lo torto e acabar errando as questões \o/
6:33 a 10:06 - Ok, já sabemos construir o diagrama. Agora: como fazer a distribuição eletrônica? Confira o exemplo na lousa com o elemento ferro. Quando você terminar de fazer a distribuição com o prof, vai perceber que último elétron desse elemento estará no 3d^6. Isso significa que este é os subnível mais energético. A camada de valência é a camada que tem o maior número na frente (nesse caso, 4s^2).
🔴 ASSISTA TAMBÉM
+ Números quânticos
+ Polaridade
❤️ REDES SOCIAIS
INSTA @cursoenemgratuito
TWITTER @enemgratuito
FACE /cursoenemgratuito/
/// AFINAL, O QUE É O CURSO ENEM GRATUITO?
Somos um canal de aulas totalmente gratuitas sobre os temas que mais caem no Enem e nos vestibulares.
Surgimos para compartilhar democraticamente conteúdos e informações sobre o Enem, ajudando você a entrar na faculdade dos seus sonhos ♥
Também temos um site com aulas escritas, questões e um plano de estudos para você se organizar!
Bora estudar com a gente?
🎓 ACESSE NOSSO CURSO 100% GRATUITO PARA O ENEM
Música da vinheta: "Summer" - Royalty Free Music from Bensound
Комментарии
 0:10:07
0:10:07
 0:13:14
0:13:14
 0:05:15
0:05:15
 0:13:06
0:13:06
 0:08:28
0:08:28
 0:19:11
0:19:11
 0:00:43
0:00:43
 0:00:53
0:00:53
 0:04:20
0:04:20
 0:09:25
0:09:25
 0:06:56
0:06:56
 0:41:30
0:41:30
 0:11:13
0:11:13
 0:06:13
0:06:13
 0:06:58
0:06:58
 0:12:21
0:12:21
 0:00:52
0:00:52
 0:00:19
0:00:19
 0:00:46
0:00:46
 0:00:24
0:00:24
 0:07:18
0:07:18
 0:00:49
0:00:49
 0:00:43
0:00:43
 0:00:50
0:00:50