filmov
tv
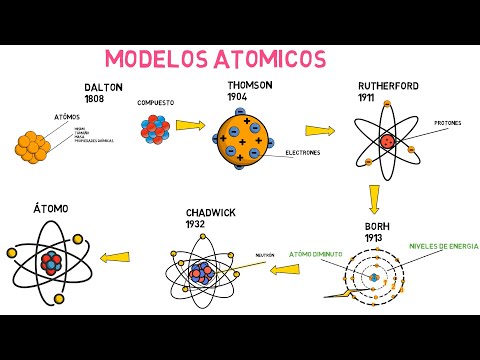
MODELOS ATÓMICOS DE THOMSON, RUTHERFORD Y BOHR | Química desde Cero

Показать описание
En este video aprenderás las características de los modelos atómicos de Thomson, Rutherford y Bohr. Se explica en consiste cada modelo, desde el más elemental hasta el más complejo de los 3. Espero que te sirva
0:00 Intro
1:39 Thomson
4:05 Rutherford
5:18 Bohr
***=====No olvides suscribirte=====***
Recuerda que me puedes encontrar en mis redes sociales:
Mis otros canales
#QuímicaDesdeCero #Química #LaQuímicaDeYamil #Suscríbete
==============================
El modelo de Thomson
El físico inglés J. J. Thomson ideó un modelo del átomo que tratase de explicar los fenómenos eléctricos. Según Thomson, el átomo sería una
esfera cargada positivamente en la cual se hallan incrustados los electrones. La carga negativa de los electrones compensaría la carga positiva, por lo que el átomo sería neutro.
¿Cómo explicaríamos el hecho de que un bolígrafo se cargue eléctricamente cuando se frota con un paño?
Según Thomson, al frotar se desprenden electrones del paño y pasan al bolígrafo, de modo que el bolígrafo queda con un exceso de electrones,
y por tanto con carga total negativa. Por el contrario, el trapo de lana, al ceder electrones, queda con exceso de protones; es decir, su carga total es positiva. Así, ambos materiales quedan electrizados; esto es, con carga eléctrica.
El modelo de Rutherford
A principios del siglo xx el físico británico (aunque nacido en Nueva Zelanda) E. Rutherford propuso otro modelo del átomo.
Según Rutherford, el átomo consta de un pequeño núcleo central cargado positivamente donde se encuentran los protones y que contiene casi toda la masa, y una parte exterior donde se hallan los electrones girando alrededor del núcleo.
El modelo de Bohr
El físico danés N. Bohr mejoró el modelo de Rutherford suponiendo que alrededor del núcleo hay diferentes capas o niveles en los que se colocan los electrones.
Según el modelo de Bohr, el átomo consta de un núcleo, que contiene protones y neutrones, y una serie de capas donde se sitúan los electrones girando alrededor del núcleo.
En el modelo de Rutherford los electrones giran describiendo órbitas que pueden estar a cualquier distancia del núcleo, pero en el modelo de Bohr los electrones solo se pueden encontrar girando en determinados niveles de energía. Se dice que el átomo de Bohr está cuantizado.
0:00 Intro
1:39 Thomson
4:05 Rutherford
5:18 Bohr
***=====No olvides suscribirte=====***
Recuerda que me puedes encontrar en mis redes sociales:
Mis otros canales
#QuímicaDesdeCero #Química #LaQuímicaDeYamil #Suscríbete
==============================
El modelo de Thomson
El físico inglés J. J. Thomson ideó un modelo del átomo que tratase de explicar los fenómenos eléctricos. Según Thomson, el átomo sería una
esfera cargada positivamente en la cual se hallan incrustados los electrones. La carga negativa de los electrones compensaría la carga positiva, por lo que el átomo sería neutro.
¿Cómo explicaríamos el hecho de que un bolígrafo se cargue eléctricamente cuando se frota con un paño?
Según Thomson, al frotar se desprenden electrones del paño y pasan al bolígrafo, de modo que el bolígrafo queda con un exceso de electrones,
y por tanto con carga total negativa. Por el contrario, el trapo de lana, al ceder electrones, queda con exceso de protones; es decir, su carga total es positiva. Así, ambos materiales quedan electrizados; esto es, con carga eléctrica.
El modelo de Rutherford
A principios del siglo xx el físico británico (aunque nacido en Nueva Zelanda) E. Rutherford propuso otro modelo del átomo.
Según Rutherford, el átomo consta de un pequeño núcleo central cargado positivamente donde se encuentran los protones y que contiene casi toda la masa, y una parte exterior donde se hallan los electrones girando alrededor del núcleo.
El modelo de Bohr
El físico danés N. Bohr mejoró el modelo de Rutherford suponiendo que alrededor del núcleo hay diferentes capas o niveles en los que se colocan los electrones.
Según el modelo de Bohr, el átomo consta de un núcleo, que contiene protones y neutrones, y una serie de capas donde se sitúan los electrones girando alrededor del núcleo.
En el modelo de Rutherford los electrones giran describiendo órbitas que pueden estar a cualquier distancia del núcleo, pero en el modelo de Bohr los electrones solo se pueden encontrar girando en determinados niveles de energía. Se dice que el átomo de Bohr está cuantizado.
Комментарии
 0:04:38
0:04:38
 0:10:55
0:10:55
 0:08:11
0:08:11
 0:10:45
0:10:45
 0:10:53
0:10:53
 0:08:31
0:08:31
 0:06:32
0:06:32
 0:06:56
0:06:56
 0:11:05
0:11:05
 0:06:59
0:06:59
 0:10:46
0:10:46
 0:02:42
0:02:42
 0:08:05
0:08:05
 0:14:56
0:14:56
 0:05:25
0:05:25
 0:13:50
0:13:50
 0:02:04
0:02:04
 0:06:46
0:06:46
 0:14:29
0:14:29
 0:09:15
0:09:15
 0:11:00
0:11:00
 0:05:14
0:05:14
 0:06:32
0:06:32
 0:00:30
0:00:30